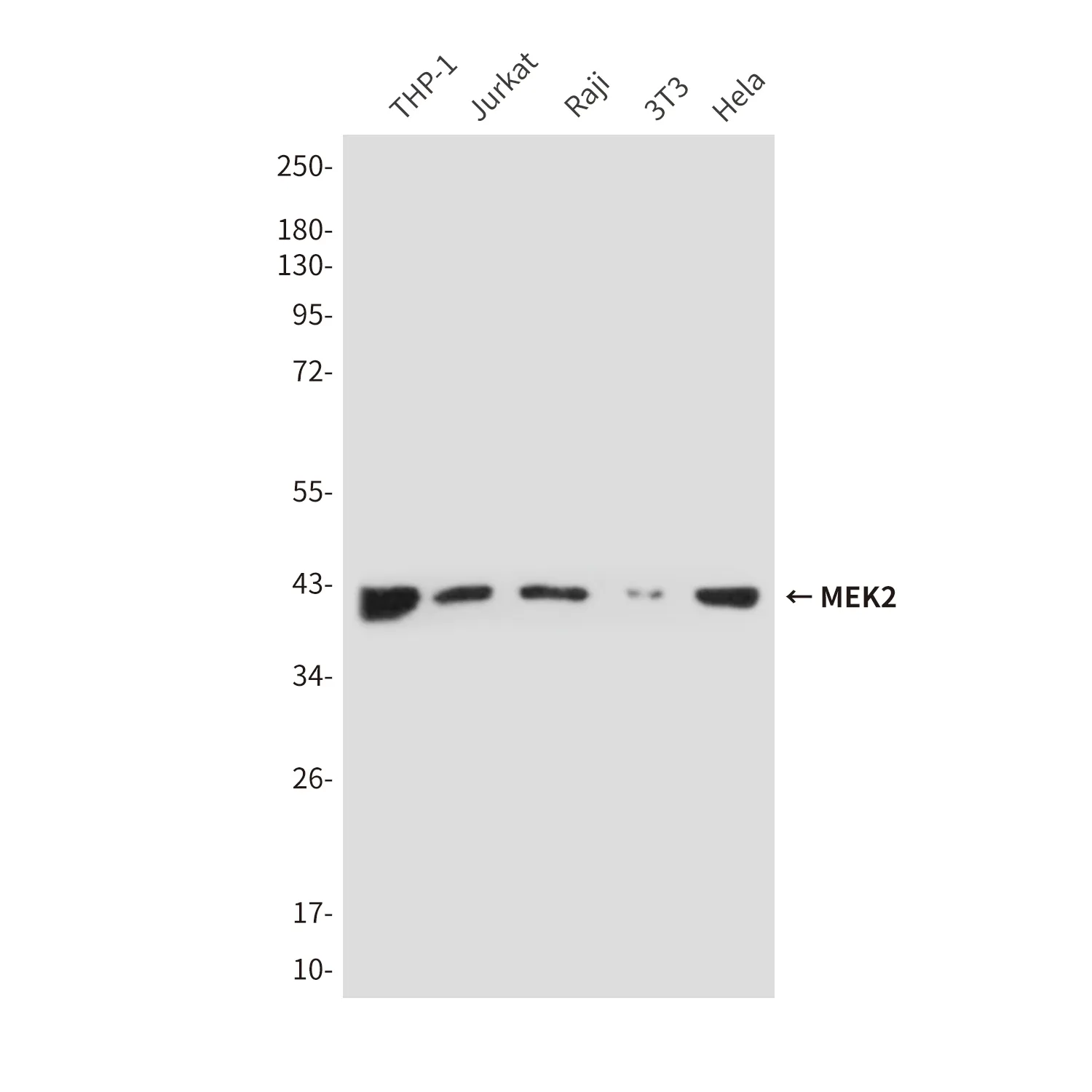
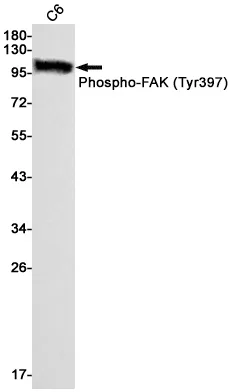
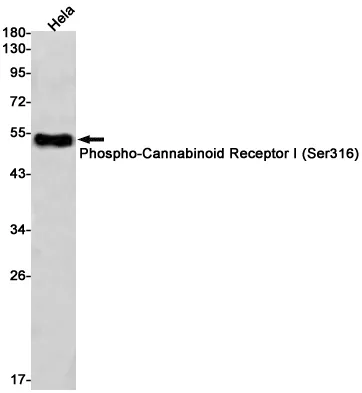
5 Lipoxygenase (15E11) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Mensch, Ratte
Genname
ALOX5
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | 5 Lipoxygenase (15E11) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Mensch, Ratte |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | ALOX5 |
| alternative Namen | ALOX5; 5-LO; 5-LOX; 5LPG; LOG5; MGC163204; LOX5; 5-lipoxygenase ; 5 Lipoxygenase; 5 LOX; ALOX 5; |
| Gene ID | 240 |
| SwissProt ID | P09917 |
| Immunogen | Ein synthetisches Peptid der humanen 5 Lipoxygenase |
Anwendung
| Anwendung | WB,IHC,ICC/IF,FC |
| Verdünnungsverhältnis | WB 1:500-1:2000,IHC 1:50-1:200,ICC/IF 1:100-1:200,FC 1:50-1:200 |
| Molekulargewicht | 78kDa |
Forschungsgebiet
| Signal Transduction; Metabolism; Energy Metabolism; Cardiovascular; Atherosclerosis; Lipoprotein metabolism; Cancer; Cancer Metabolism; Metabolic signaling pathway; Hormone biosynthesis; Pathways and Processes; Metabolic signaling pathways; Lipid and lipoprotein metabolism; Lipoprotein metabolism; Energy transfer pathways; Energy Metabolism; Endocrine metabolism; Hormone biosynthesis; Types of disease; Cancer; Heart disease |
Hintergrund
| Katalysiert den ersten Schritt der Leukotrienbiosynthese und spielt dadurch eine Rolle bei Entzündungsprozessen. Katalysiert die Oxygenierung von Arachidonat ((5Z,8Z,11Z,14Z)-Eicosatetraenoat) zu 5-Hydroperoxyeicosatetraenoat (5-HPETE) gefolgt von der Dehydratisierung zu 5,6-Epoxyeicosatetraenoat (Leukotrien A4/LTA4), den ersten beiden Schritten in der Biosynthese von Leukotrienen, die starke Mediatoren der Entzündung sind (PubMed:8631361, PubMed:21233389, PubMed:22516296, PubMed:24282679, PubMed:19022417, PubMed:23246375, PubMed:8615788, PubMed:24893149, PubMed:31664810). Es katalysiert außerdem die Oxygenierung von Arachidonat zu 8-Hydroperoxyicosatetraenoat (8-HPETE) und 12-Hydroperoxyicosatetraenoat (12-HPETE) (PubMed:23246375). Es weist Lipoxin-Synthase-Aktivität auf und kann (15S)-HETE in ein konjugiertes Tetraen umwandeln (PubMed:31664810). Obwohl Arachidonsäure das bevorzugte Substrat ist, kann dieses Enzym auch oxidierte Fettsäuren, die von Arachidonsäure abgeleitet sind, wie (15S)-HETE, Eicosapentaensäure (EPA) wie (18R)- und (18S)-HEPE oder Docosahexaensäure (DHA) metabolisieren. Dies führt zur Bildung der spezialisierten pro-resolvierenden Mediatoren (SPM) Lipoxin und Resolvin E bzw. D. Daher ist es an entzündungshemmenden Reaktionen beteiligt (PubMed:21206090, PubMed:31664810, PubMed:8615788, PubMed:17114001, PubMed:32404334). Die Oxidation von DHA hemmt direkt die Proliferation von Endothelzellen und die sprossende Angiogenese über den Peroxisomenproliferator-aktivierten Rezeptor gamma (PPARgamma) (durch Ähnlichkeit). Es katalysiert weder die Oxygenierung von Linolsäure noch wandelt es (5S)-HETE in Lipoxin-Isomere um (PubMed:31664810). Neben Entzündungsprozessen ist es an der Migration dendritischer Zellen und der Wundheilung über einen antioxidativen Mechanismus beteiligt, der auf der Regulation der Hämoxygenase-1 (HO-1)-Expression beruht. Zudem beeinflusst es die Adhäsion von Monozyten an das Endothel durch die Expression von ITGAM auf Monozyten (ähnlich). Darüber hinaus trägt es zum Aufbau einer adaptiven humoralen Immunität bei, indem es primäre ruhende B-Zellen und follikuläre T-Helferzellen reguliert. Es ist an der CD40-induzierten Produktion reaktiver Sauerstoffspezies (ROS) nach CD40-Bindung in B-Zellen beteiligt, indem es mit PIK3R1 interagiert, welches ALOX5 mit CD40 verbindet (PubMed:21200133). Möglicherweise spielt es auch eine Rolle in der Glukosehomöostase, der Regulation der Insulinsekretion und der durch Palmitinsäure induzierten Insulinresistenz über AMPK (ähnlich). Kann die Knochenmineralisierung und die Differenzierung von Fettzellen in induzierten pluripotenten Stammzellen regulieren (durch Ähnlichkeit). |