ADAR1 (16R16) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Menschlich
Genname
ADAR
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | ADAR1 (16R16) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Menschlich |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | ADAR |
| alternative Namen | ADAR; Adar1; AGS6; DRADA; Dsh; Dsrad; IFI4; P136; |
| Gene ID | 103 |
| SwissProt ID | P55265 |
| Immunogen | Ein synthetisches Peptid des humanen ADAR1 |
Anwendung
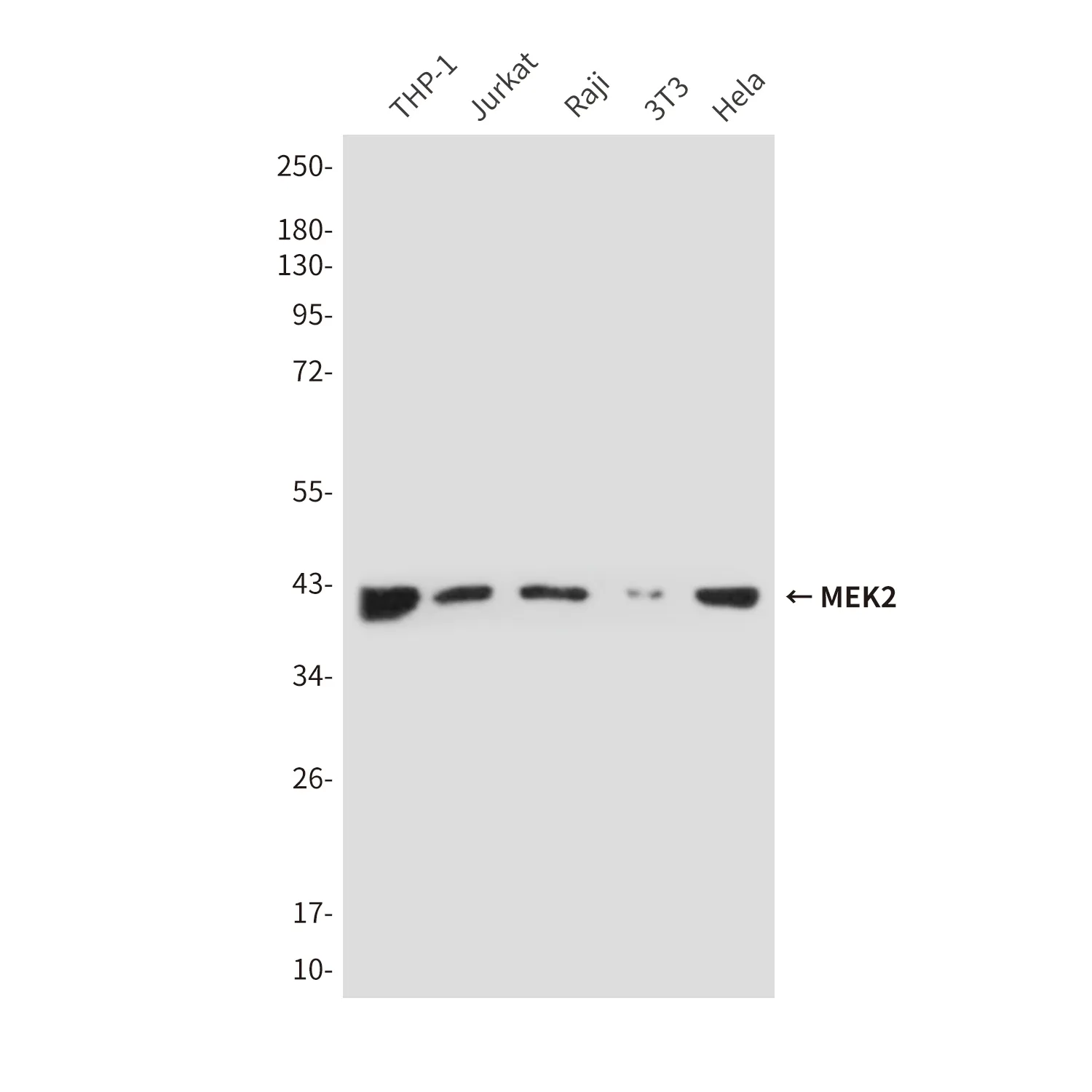
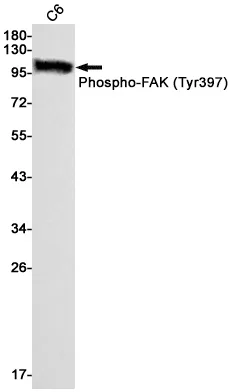
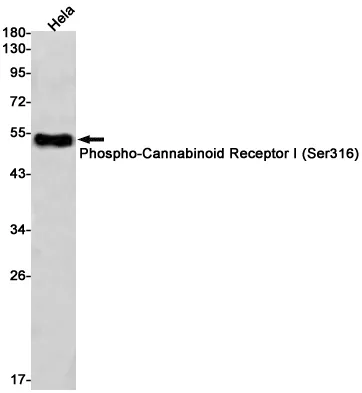
| Anwendung | WB,IHC,FC,IF-P |
| Verdünnungsverhältnis | WB 1:1000-1:5000,IHC 1:50-1:100,FC 1:10-1:100,IF-P 1:50-1:100 |
| Molekulargewicht | 136kDa |
Forschungsgebiet
| Microbiology |
Hintergrund
| Es wandelt mehrere Adenosine in Inosine um und erzeugt I/U-Fehlpaarungen in doppelsträngigen RNA-Substraten ohne erkennbare Sequenzspezifität. Es katalysiert die hydrolytische Desaminierung von Adenosin zu Inosin in doppelsträngiger RNA (dsRNA), ein Vorgang, der als A-zu-I-RNA-Editierung bezeichnet wird (PubMed:7972084, PubMed:7565688, PubMed:12618436). Dies kann die Genexpression und -funktion auf vielfältige Weise beeinflussen, darunter die mRNA-Translation durch Veränderung von Codons und damit der Aminosäuresequenz von Proteinen; das prä-mRNA-Splicing durch Veränderung von Spleißstellen-Erkennungssequenzen; die RNA-Stabilität durch Veränderung von Sequenzen, die an der Nukleaseerkennung beteiligt sind; die genetische Stabilität im Falle von RNA-Virusgenomen durch Veränderung von Sequenzen während der viralen RNA-Replikation; und RNA-strukturabhängige Aktivitäten wie die Produktion oder das Targeting von microRNA oder Protein-RNA-Interaktionen. Kann sowohl virale als auch zelluläre RNA editieren und RNA an mehreren Stellen (Hyper-Editing) oder an spezifischen Stellen (ortsspezifisches Editing) verändern. Zu seinen zellulären RNA-Substraten gehören das Blasenkrebs-assoziierte Protein (BLCAP), die Neurotransmitterrezeptoren für Glutamat (GRIA2) und Serotonin (HTR2C) sowie der GABA-Rezeptor (GABRA3). Das ortsspezifische RNA-Editing von Transkripten, die für diese Proteine kodieren, führt zu Aminosäuresubstitutionen, wodurch sich deren funktionelle Aktivität verändert. Es zeigt ein geringes Editing-Niveau an der GRIA2-Q/R-Stelle, editiert jedoch effizient an der R/G-Stelle und an HOTSPOT1. Zu seinen viralen RNA-Substraten gehören das Hepatitis-C-Virus (HCV), das Vesikuläre Stomatitis-Virus (VSV), das Masernvirus (MV), das Hepatitis-Delta-Virus (HDV) und das Humane Immundefizienz-Virus Typ 1 (HIV-1). Zeigt entweder eine provirale (HDV, MV, VSV und HIV-1) oder eine antivirale Wirkung (HCV), die editierungsabhängig (HDV und HCV), editierungsunabhängig (VSV und MV) oder beides (HIV-1) sein kann. Beeinträchtigt die HCV-Replikation durch RNA-Editierung an mehreren Stellen. Fördert die Replikation von MV, VSV und HIV-1 durch einen editierungsunabhängigen Mechanismus über die Suppression der Aktivierung und Funktion von EIF2AK2/PKR. Stimuliert sowohl die Freisetzung als auch die Infektiosität von HIV-1-Viruspartikeln durch einen editierungsabhängigen Mechanismus, indem es mit viralen RNAs interagiert und Adenosine in der 5'-UTR sowie in der Rev- und Tat-kodierenden Sequenz editiert. ADAR1 kann die Virusreplikation von HDV durch A-zu-I-Editierung an einer als Amber/W bezeichneten Stelle steigern. Dabei wird ein UAG-Amber-Stoppcodon in ein UIG-Tryptophan-(W)-Codon umgewandelt, was die Synthese des großen Delta-Antigens (L-HDAg) ermöglicht, welches eine Schlüsselrolle bei der Assemblierung der Viruspartikel spielt. Hohe ADAR1-Konzentrationen hemmen jedoch die HDV-Replikation. |