AHA1 (3L10) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Mensch, Maus, Ratte
Genname
AHSA1
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | AHA1 (3L10) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Mensch, Maus, Ratte |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | AHSA1 |
| alternative Namen | AHA 1; AHA1; AHSA 1; Ahsa1; C14orf3; HSPC322; p38; |
| Gene ID | 10598 |
| SwissProt ID | O95433 |
| Immunogen | Ein synthetisches Peptid des menschlichen AHA1 |
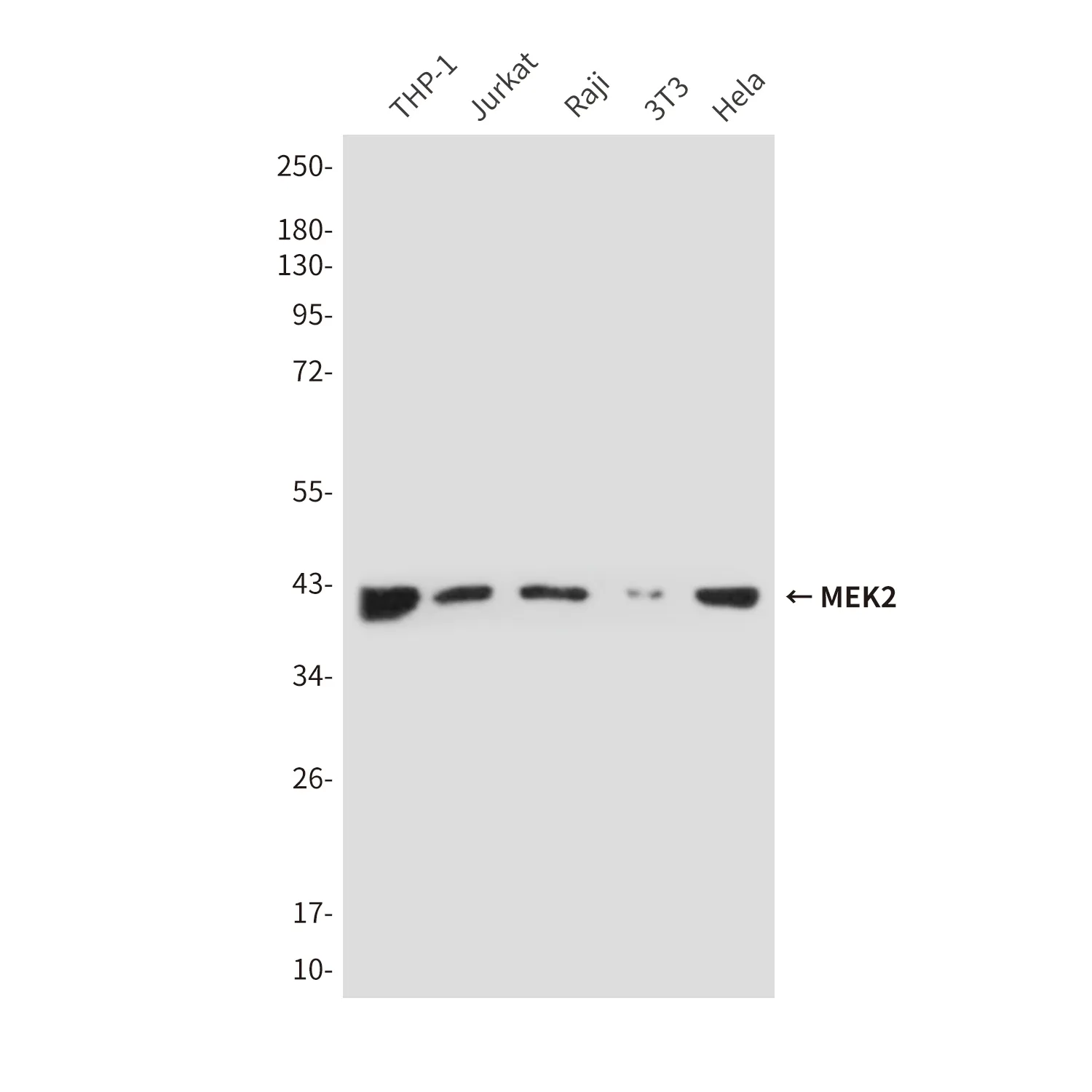
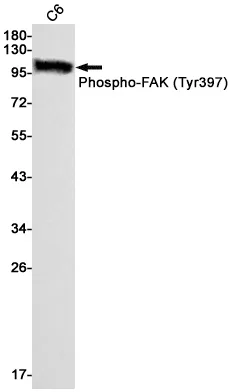
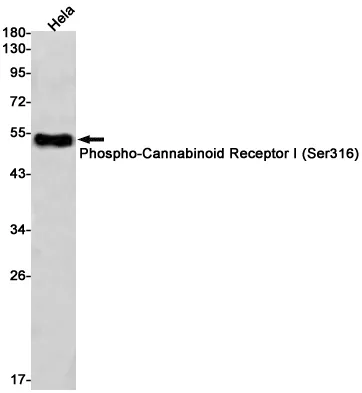
Anwendung
| Anwendung | WB,IP |
| Verdünnungsverhältnis | WB 1:1000-1:5000,IP 1:20-1:50 |
| Molekulargewicht | 38kDa |
Forschungsgebiet
| Signal Transduction |
Hintergrund
| Ein Co-Chaperon, das die ATPase-Aktivität von HSP90 stimuliert (durch Ähnlichkeit). Es kann einen Schritt im Transport vom endoplasmatischen Retikulum zum Golgi-Apparat beeinflussen. Es fungiert als Co-Chaperon von HSP90AA1 (PubMed:29127155). Es aktiviert die ATPase-Aktivität von HSP90AA1 und erhöht dadurch dessen Chaperon-Aktivität (PubMed:29127155). Es konkurriert mit dem inhibitorischen Co-Chaperon FNIP1 um die Bindung an HSP90AA1 und stellt somit einen reziproken Regulationsmechanismus für das Chaperoning von Client-Proteinen dar (PubMed:27353360). Es konkurriert außerdem mit dem inhibitorischen Co-Chaperon TSC1 um die Bindung an HSP90AA1 und stellt somit ebenfalls einen reziproken Regulationsmechanismus für das Chaperoning von Client-Proteinen dar (PubMed:29127155). |