CYP27A1 (5H15) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Mensch, Maus, Ratte
Genname
CYP27A1
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | CYP27A1 (5H15) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Mensch, Maus, Ratte |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | CYP27A1 |
| alternative Namen | CP27; CTX; CYP; CYP27; CYP27A1; |
| Gene ID | 1593 |
| SwissProt ID | Q02318 |
| Immunogen | Ein synthetisches Peptid des humanen CYP27A1 |
Anwendung
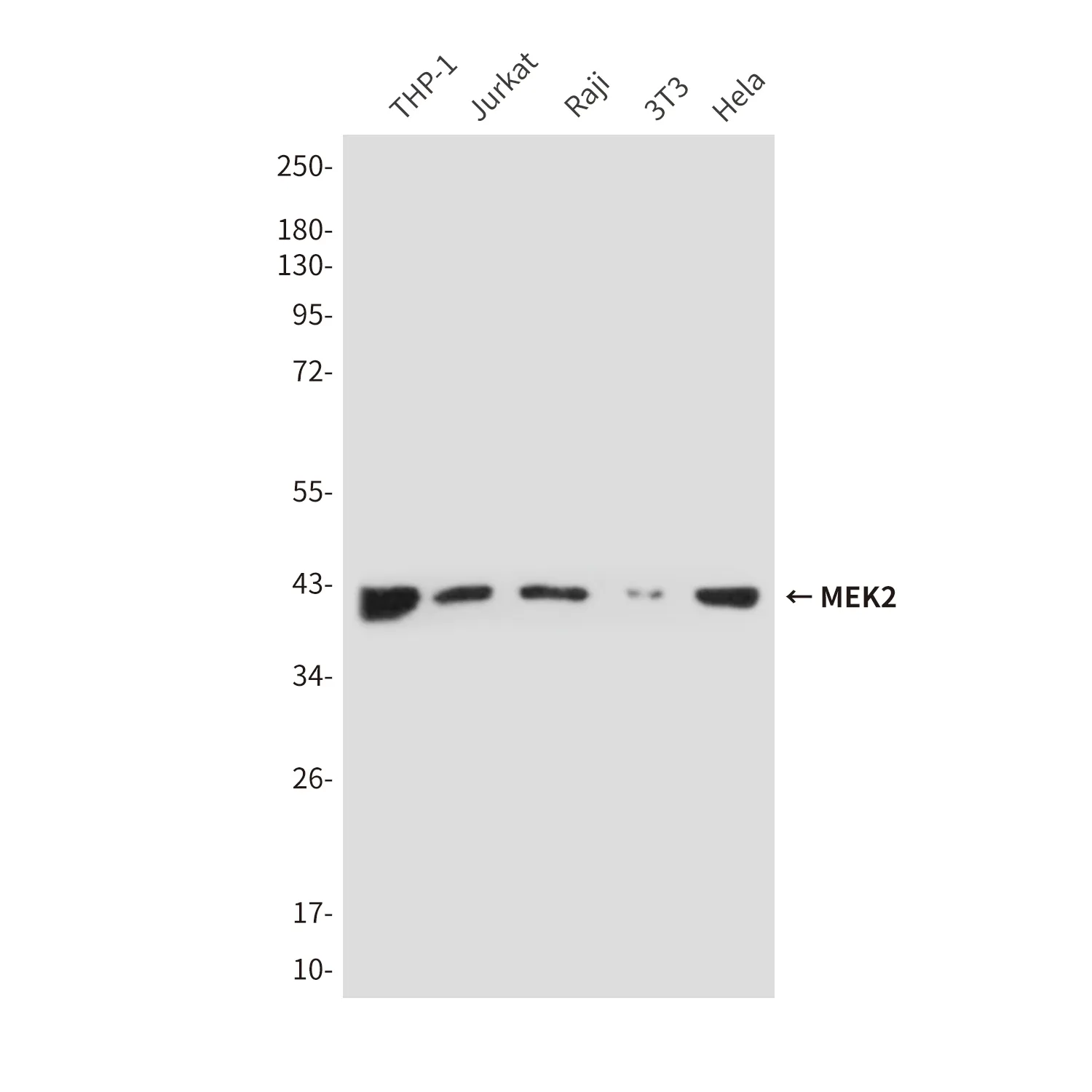
| Anwendung | WB,IHC,ICC/IF,FC |
| Verdünnungsverhältnis | WB 1:1000-1:5000,IHC 1:100-1:200,ICC/IF 1:50-1:100,FC 1:50-1:200 |
| Molekulargewicht | 60kDa |
Forschungsgebiet
| Cardiovascular |
Hintergrund
| Katalysiert den ersten Schritt der Oxidation der Seitenkette von Sterol-Zwischenprodukten; die 27-Hydroxylierung von 5-β-Cholestan-3-α,7-α,12-α-triol. Besitzt außerdem Vitamin-D3-25-Hydroxylase-Aktivität. Cytochrom-P450-Monooxygenase, die die regio- und stereospezifische Hydroxylierung von Cholesterin und seinen Derivaten katalysiert. Hydroxyliert (mit R-Stereochemie) die terminale Methylgruppe der Cholesterin-Seitenkette in einer dreistufigen Reaktion, wobei zunächst ein C26-Alkohol, dann ein C26-Aldehyd und schließlich eine C26-Säure entsteht (PubMed:9660774, PubMed:12077124, PubMed:21411718, PubMed:28190002). Reguliert die Cholesterinhomöostase durch Katalyse der Umwandlung von überschüssigem Cholesterin in Gallensäuren über den „neutralen“ (klassischen) und den „sauren“ (alternativen) Stoffwechselweg (PubMed:9660774, PubMed:1708392, PubMed:11412116, PubMed:2019602, PubMed:7915755, PubMed:9186905, PubMed:9790667). Möglicherweise reguliert es die Cholesterinhomöostase auch durch die Bildung aktiver Oxysterole, die als Liganden für die nukleären Rezeptoren NR1H2 und NR1H3 fungieren und die Transkription von Genen des Lipidstoffwechsels modulieren (PubMed:9660774, PubMed:12077124). Es spielt eine Rolle im Cholestanolstoffwechsel des Kleinhirns. Ähnlich wie Cholesterin hydroxyliert es Cholestanol und kann die Diffusion von Sterolen durch die Blut-Hirn-Schranke in den systemischen Kreislauf zur weiteren Degradation erleichtern (PubMed:28190002). Es hydroxyliert außerdem retinales 7-Ketocholesterol, ein schädliches Oxysterol mit proinflammatorischen und proapoptotischen Wirkungen, und könnte an dessen Elimination aus dem retinalen Pigmentepithel beteiligt sein (PubMed:21411718). Möglicherweise spielt es eine redundante Rolle in der Vitamin-D-Biosynthese. Es katalysiert die 25-Hydroxylierung von Vitamin D3, die für dessen Umwandlung in eine funktionell aktive Form erforderlich ist (PubMed:15465040). |