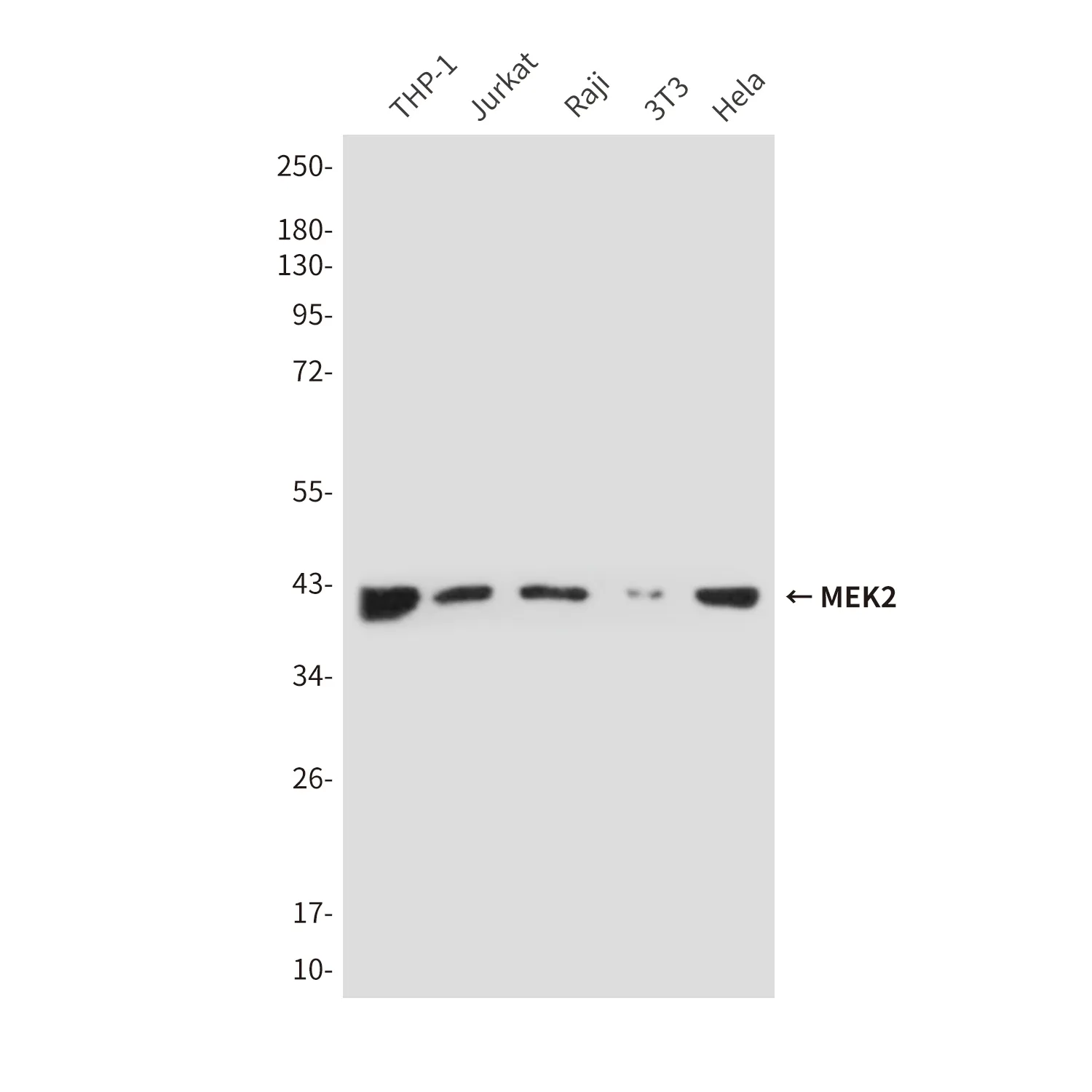
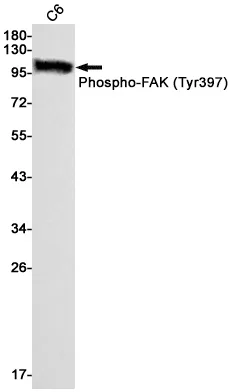
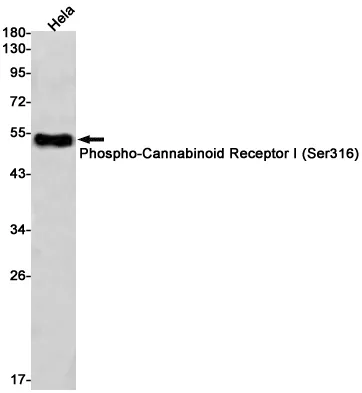
Cytochrom P450 1A2 (8B7) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Menschlich
Genname
CYP1A2
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | Cytochrom P450 1A2 (8B7) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Menschlich |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | CYP1A2 |
| alternative Namen | CP12; CYP1A2; CYPIA2; P3 450; P450 4; P450 P3; |
| Gene ID | 1544 |
| SwissProt ID | P05177 |
| Immunogen | Ein synthetisches Peptid des humanen Cytochrom P450 1A2 |
Anwendung
| Anwendung | WB,ICC/IF,FC |
| Verdünnungsverhältnis | WB 1:1000-1:5000,ICC/IF 1:200-1:500,FC 1:50-1:200 |
| Molekulargewicht | 58kDa |
Forschungsgebiet
| Caffeine metabolism;Tryptophan metabolism;Linoleic acid metabolism;Retinol metabolism;Metabolism of xenobiotics by cytochrome P450;Drug metabolism; |
Hintergrund
| Cytochrome P450 sind eine Gruppe von Häm-Thiolat-Monooxygenasen. In Lebermikrosomen ist dieses Enzym an einem NADPH-abhängigen Elektronentransportweg beteiligt. Eine Cytochrom-P450-Monooxygenase ist am Stoffwechsel verschiedener endogener Substrate beteiligt, darunter Fettsäuren, Steroidhormone und Vitamine (PubMed:9435160, PubMed:10681376, PubMed:11555828, PubMed:12865317, PubMed:19965576). Mechanistisch nutzt das Enzym molekularen Sauerstoff, indem es ein Sauerstoffatom in ein Substrat einfügt und das zweite zu einem Wassermolekül reduziert. Dabei werden zwei Elektronen von NADPH über Cytochrom-P450-Reduktase (NADPH-Hämoprotein-Reduktase) bereitgestellt (PubMed:9435160, PubMed:10681376, PubMed:11555828, PubMed:12865317, PubMed:19965576). Es katalysiert die Hydroxylierung von Kohlenstoff-Wasserstoff-Bindungen (PubMed:11555828, PubMed:12865317). Es zeigt eine hohe katalytische Aktivität bei der Bildung von Hydroxyöstrogenen aus Östron (E1) und 17β-Östradiol (E2), nämlich 2-Hydroxy-E1 und -E2 (PubMed:11555828, PubMed:12865317). Metabolisiert Cholesterin zu 25-Hydroxycholesterin, einem physiologischen Regulator der zellulären Cholesterinhomöostase (PubMed:21576599). Es fungiert möglicherweise als wichtiges Enzym für die all-trans-Retinsäure-Biosynthese in der Leber. Es katalysiert zwei aufeinanderfolgende oxidative Umwandlungen von all-trans-Retinol zu all-trans-Retinal und anschließend zur aktiven Form, der all-trans-Retinsäure (PubMed:10681376). Es katalysiert primär die stereoselektive Epoxidierung der letzten Doppelbindung von mehrfach ungesättigten Fettsäuren (PUFA) und zeigt dabei eine starke Präferenz für das (R,S)-Stereoisomer (PubMed:19965576). Es katalysiert die bisallylische Hydroxylierung und die Omega-1-Hydroxylierung von PUFA (PubMed:9435160). Kann auch am Eicosanoid-Stoffwechsel beteiligt sein, indem es Hydroperoxid-Spezies in Oxo-Metabolite umwandelt (Lipoxygenase-ähnliche Reaktion, NADPH-unabhängig) (PubMed:21068195). Spielt eine Rolle im oxidativen Metabolismus von Xenobiotika. Katalysiert die N-Hydroxylierung heterocyclischer Amine und die O-Deethylierung von Phenacetin (PubMed:14725854). Metabolisiert Koffein wahrscheinlich über N3-Demethylierung. |