FAP1 (17O11) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Mensch, Maus
Genname
FAP
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | FAP1 (17O11) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Mensch, Maus |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | FAP |
| alternative Namen | 170 kDa melanoma membrane bound gelatinase; DPPIV; FAP; FAPA; Seprase; |
| Gene ID | 2191 |
| SwissProt ID | Q12884 |
| Immunogen | Rekombinantes Protein des humanen Fibroblasten-Aktivierungsproteins,alpha |
Anwendung
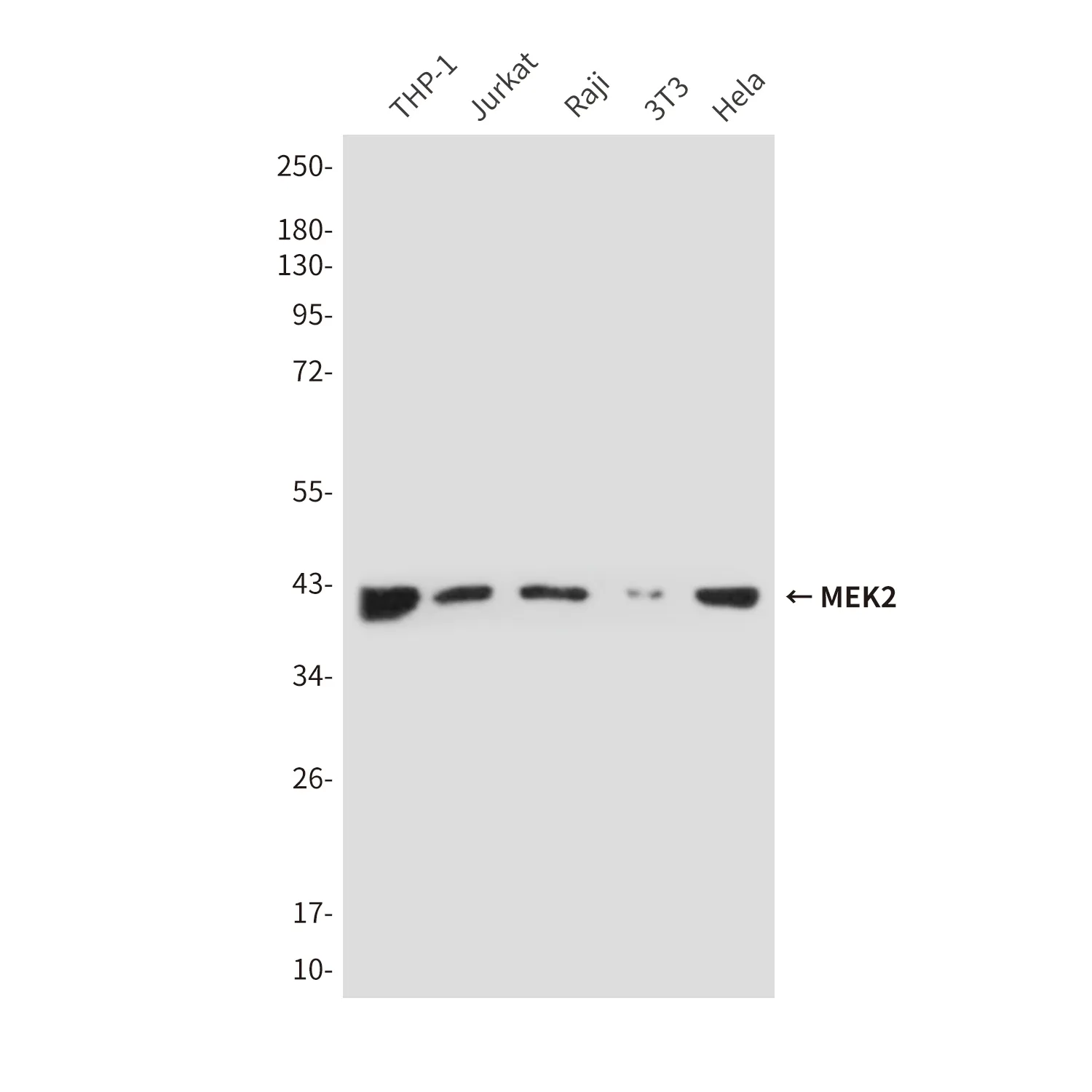
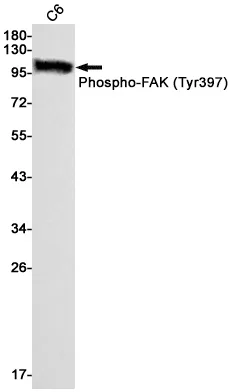
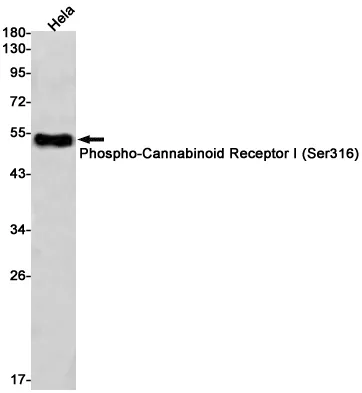
| Anwendung | WB,IHC,IF-P |
| Verdünnungsverhältnis | WB 1:500-1:2000,IHC 1:100-1:200,IF-P 1:100-1:200 |
| Molekulargewicht | 88kDa |
Forschungsgebiet
| Cell Biology |
Hintergrund
| In Verbindung mit DPP4 ist es an der perizellulären Proteolyse der extrazellulären Matrix (ECM) sowie an der Migration und Invasion von Endothelzellen in die ECM beteiligt. Es spielt möglicherweise eine Rolle bei der Geweberegeneration während der Entwicklung und der Wundheilung und trägt zur Invasivität maligner Tumoren bei. Es handelt sich um eine Serinprotease auf Zelloberflächenebene, die am Abbau der extrazellulären Matrix beteiligt ist und an zahlreichen zellulären Prozessen wie Geweberegeneration, Fibrose, Wundheilung, Entzündung und Tumorwachstum mitwirkt. Sowohl die Plasmamembran- als auch die löslichen Formen weisen eine post-Prolin-spaltende Endopeptidase-Aktivität auf, mit einer deutlichen Präferenz für Ala/Ser-Gly-Pro-Ser/Asn/Ala-Konsekutivsequenzen auf Substraten wie alpha-2-Antiplasmin SERPINF2 und SPRY2 (PubMed:14751930, PubMed:16223769, PubMed:16480718, PubMed:16410248, PubMed:17381073, PubMed:18095711, PubMed:21288888, PubMed:24371721). Sie bauen auch Gelatine und hitzedenaturiertes Kollagen Typ I ab, jedoch nicht natives Kollagen Typ I und IV, Vitronectin, Tenascin, Laminin, Fibronektin, Fibrin oder Casein (PubMed:9065413, PubMed:2172980, PubMed:7923219, PubMed:10347120, PubMed:10455171, PubMed:12376466, PubMed:16223769, PubMed:16651416, PubMed:18095711). Besitzt außerdem Dipeptidylpeptidase-Aktivität und ist in der Lage, die Prolylbindung zwei Reste vom N-Terminus synthetischer Dipeptidsubstrate zu hydrolysieren, vorausgesetzt, der vorletzte Rest ist Prolin, wobei eine Präferenz für Ala-Pro, Ile-Pro, Gly-Pro, Arg-Pro und Pro-Pro besteht (PubMed:10347120, PubMed:10593948, PubMed:16175601, PubMed:16223769, PubMed:16651416, PubMed:16410248, PubMed:17381073, PubMed:21314817, PubMed:24371721, PubMed:24717288). Natürliche Neuropeptidhormone für Dipeptidylpeptidase sind Neuropeptid Y (NPY), Peptid YY (PYY), Substanz P (TAC1) und das natriuretische Peptid des Gehirns 32 (NPPB) (PubMed:21314817). Die Plasmamembranform ist in Verbindung mit DPP4, PLAUR oder Integrinen an der perizellulären Proteolyse der extrazellulären Matrix (ECM) beteiligt und fördert dadurch Zelladhäsion, -migration und -invasion durch die ECM. Sie spielt eine Rolle bei der Geweberegeneration während der Entwicklung und Wundheilung. Sie trägt zur Zellinvasion in die ECM bei malignen Melanomen bei. Sie verstärkt das Tumorwachstum durch Steigerung der Angiogenese, des Kollagenfaserabbaus und der Apoptose sowie durch Reduzierung der Antitumorantwort des Immunsystems. Sie fördert die Invasion von Gliomzellen durch das Hirnparenchym durch den Abbau des Proteoglykans Brevican. Wirkt als Tumorsuppressor in melanozytären Zellen durch Regulierung der Zellproliferation und des Zellüberlebens auf eine von der Serinproteaseaktivität unabhängige Weise. |