Insulinrezeptor (13M3) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Menschlich
Genname
INSR
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | Insulinrezeptor (13M3) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Menschlich |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Geliefert in 50 mM Tris-Glycin (pH 7,4), 0,15 M NaCl, 40 % Glycerin, 0,01 % Konservierungsmittel N (neuer Typ) und 0,05 % Schutzprotein. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | INSR |
| alternative Namen | CD220; HHF5; human insulin receptor; Insr; Insulin receptor subunit beta; IR 1; IR; |
| Gene ID | 3643 |
| SwissProt ID | P06213 |
| Immunogen | Ein synthetisches Peptid des humanen Insulinrezeptors beta |
Anwendung
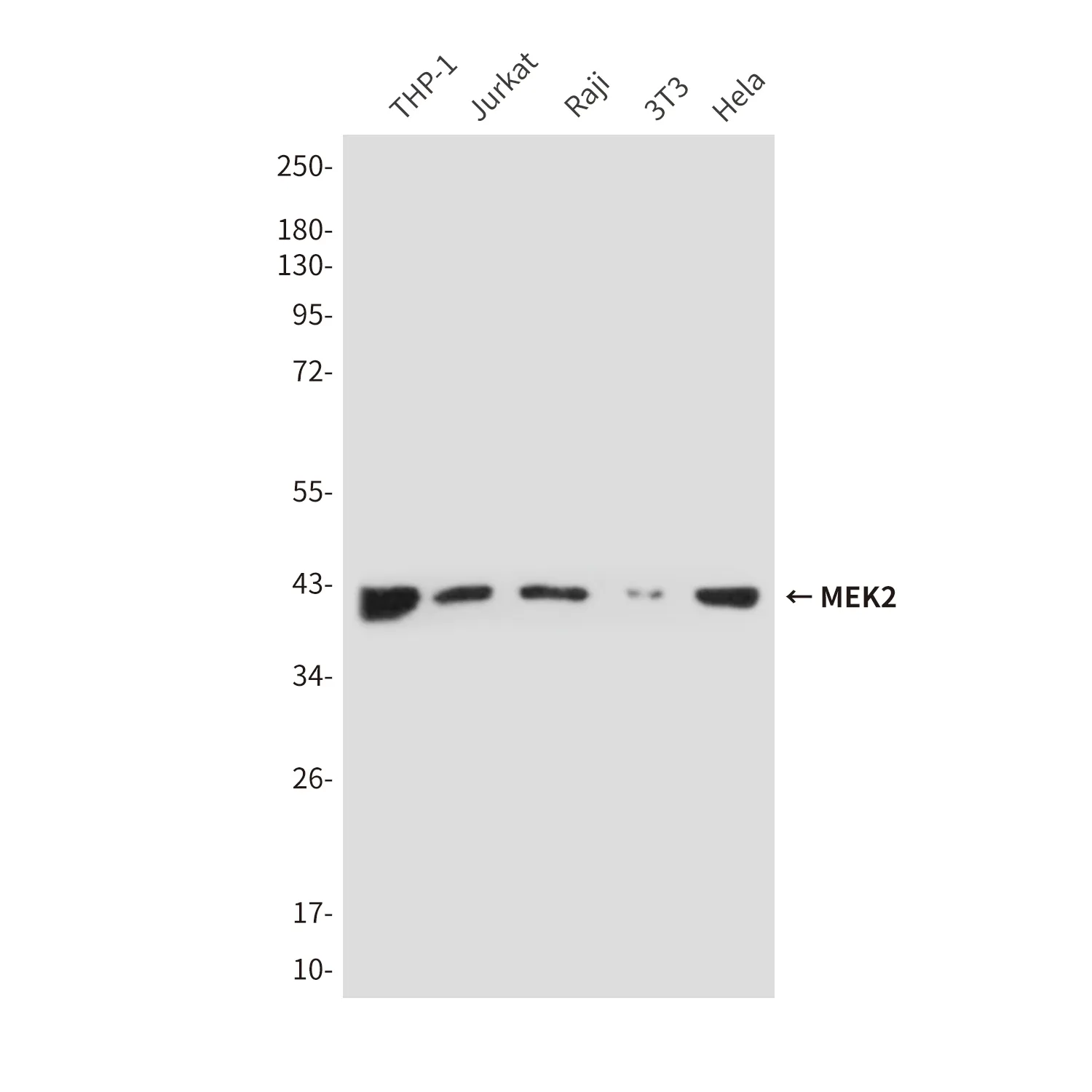
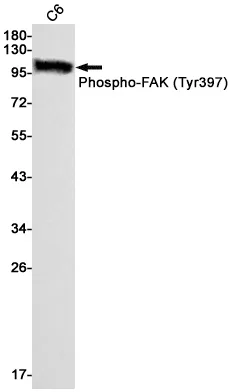
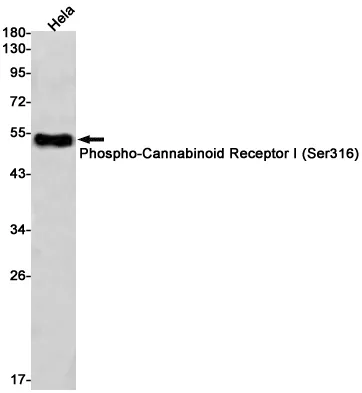
| Anwendung | WB,IHC,IP,IF-P |
| Verdünnungsverhältnis | WB 1:500-1:2000,IHC 1:200-1:500,IP 1:20-1:50,IF-P 1:200-1:500 |
| Molekulargewicht | 156kDa |
Forschungsgebiet
| Regulation of Actin Dynamics; Insulin Receptor; AMPK; Adherens_Junction |
Hintergrund
| Der Insulinrezeptor ist eine Transmembran-Rezeptor-Tyrosinkinase, die in vielen Zelllinien und Zelltypen fetaler und postnataler Gewebe weit verbreitet exprimiert wird. Die Bindung von Insulin an den IR induziert die Phosphorylierung intrazellulärer Tyrosinkinasedomänen und die Rekrutierung mehrerer intrazellulärer Proteine mit SH2- und SH3-Domänen, die als Signalintermediäre für die pleiotropen Wirkungen von Insulin dienen. Die Insulinbindung führt zur Phosphorylierung verschiedener intrazellulärer Substrate, darunter Insulinrezeptorsubstrate (IRS1, 2, 3, 4), SHC, GAB1, CBL und weitere Signalintermediäre. Jedes dieser phosphorylierten Proteine dient als Andockstelle für andere Signalproteine mit Src-Homologie-2-Domänen (SH2-Domäne), die spezifisch verschiedene Phosphotyrosinreste erkennen, darunter die regulatorische p85-Untereinheit der PI3K und SHP2. Die Phosphorylierung von IRS-Proteinen führt zur Aktivierung zweier Hauptsignalwege: des PI3K-AKT/PKB-Signalwegs, der für die meisten metabolischen Wirkungen von Insulin verantwortlich ist, und des Ras-MAPK-Signalwegs, der die Expression einiger Gene reguliert und mit dem PI3K-Signalweg zusammenwirkt, um Zellwachstum und -differenzierung zu steuern. Die Bindung der SH2-Domänen der PI3K an Phosphotyrosine auf IRS1 führt zur Aktivierung der PI3K und zur Bildung von Phosphatidylinositol-(3,4,5)-triphosphat (PIP3), einem Lipid-Second-Messenger, der verschiedene PIP3-abhängige Serin/Threonin-Kinasen wie PDPK1 und anschließend AKT/PKB aktiviert. Der Nettoeffekt dieses Signalwegs ist die Translokation des Glukosetransporters SLC2A4/GLUT4 aus zytoplasmatischen Vesikeln zur Zellmembran, um den Glukosetransport zu ermöglichen. Darüber hinaus ist der aktivierte AKT/PKB-Signalweg nach Insulin-Stimulation für Folgendes verantwortlich: die antiapoptotische Wirkung von Insulin durch Induktion der BAD-Phosphorylierung; die Regulation der Expression gluconeogener und lipogener Enzyme durch Kontrolle der Aktivität der FOX-Transkriptionsfaktoren (Winged Helix or Forkhead). Ein weiterer durch die PI3K-AKT/PKB-Aktivierung regulierter Signalweg ist der mTORC1-Signalweg, der Zellwachstum und -stoffwechsel reguliert und Insulinsignale integriert. AKT vermittelt die insulininduzierte Proteinsynthese durch Phosphorylierung von TSC2 und aktiviert dadurch den mTORC1-Signalweg. Der Ras/RAF/MAP2K/MAPK-Signalweg ist hauptsächlich an der Vermittlung von Zellwachstum, Überleben und Zelldifferenzierung durch Insulin beteiligt. Phosphoryliertes IRS1 rekrutiert den GRB2/SOS-Komplex, der die Aktivierung des Ras/RAF/MAP2K/MAPK-Signalwegs auslöst. Neben Insulin kann der Insulinrezeptor auch insulinähnliche Wachstumsfaktoren (IGF-I und IGF-II) binden. Die kurze Isoform weist eine höhere Affinität zur IGFII-Bindung auf. In einem Hybridrezeptor mit IGF1R bindet sie IGF1. PubMed:12138094 zeigt, dass Hybridrezeptoren aus IGF1R und der langen INSR-Isoform mit hoher Affinität durch IGF1, mit geringer Affinität durch IGF2 und nicht signifikant durch Insulin aktiviert werden. Hybridrezeptoren aus IGF1R und der kurzen INSR-Isoform werden hingegen durch IGF1, IGF2 und Insulin aktiviert. Im Gegensatz dazu zeigt PubMed:16831875, dass Hybridrezeptoren aus IGF1R und der langen sowie aus IGF1R und der kurzen INSR-Isoform ähnliche Bindungseigenschaften aufweisen: Beide binden IGF1 und haben eine geringe Affinität zu Insulin. In Adipozyten hemmt sie die Lipolyse (aufgrund ähnlicher Eigenschaften). |