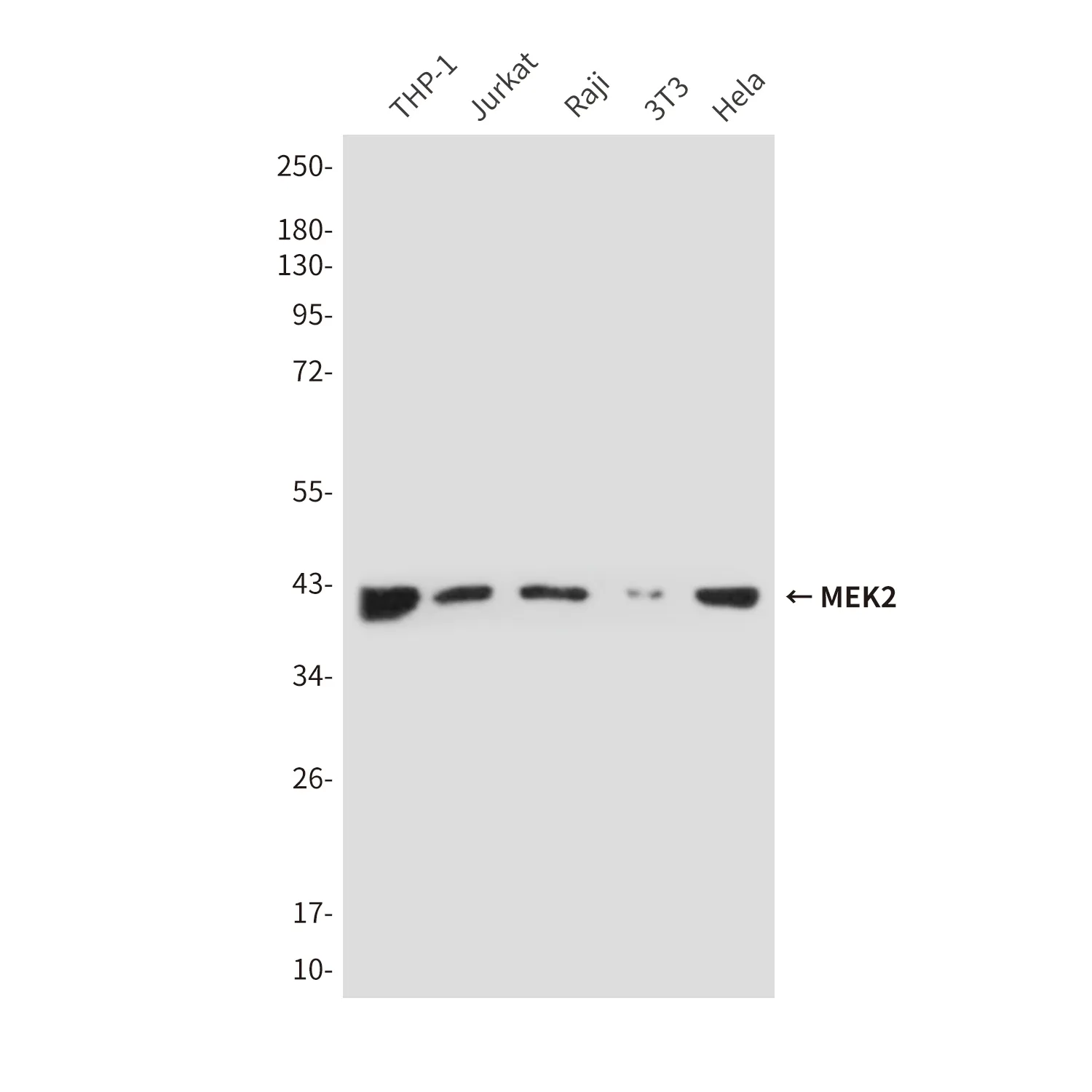
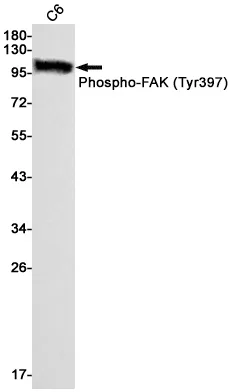
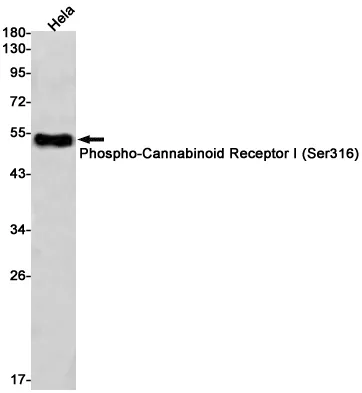
OGT (19A13) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Mensch, Maus, Ratte
Genname
OGT
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | OGT (19A13) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Mensch, Maus, Ratte |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Geliefert in 50 mM Tris-Glycin (pH 7,4), 0,15 M NaCl, 40 % Glycerin, 0,01 % Konservierungsmittel N (neuer Typ) und 0,05 % Schutzprotein. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | OGT |
| alternative Namen | HRNT1; O-GLCNAC; |
| Gene ID | 8473 |
| SwissProt ID | O15294 |
| Immunogen | Ein synthetisches Peptid der humanen OGT/O-verknüpften N-Acetylglucosamin-Transferase |
Anwendung
| Anwendung | WB,IHC,ICC/IF,FC |
| Verdünnungsverhältnis | WB 1:500-1:2000,IHC 1:20-1:50,ICC/IF 1:20-1:100,FC 1:20-1:50 |
| Molekulargewicht | 117kDa |
Forschungsgebiet
| Neuroscience |
Hintergrund
| Die Anlagerung von Nukleotid-aktivierten Zuckern an das Polypeptid erfolgt über eine O-glykosidische Bindung mit der Hydroxylgruppe von Serin oder Threonin. Dies vermittelt die O-Glykosylierung von MLL5 und HCFC1 und fördert die proteolytische Reifung von HCFC1. Zudem katalysiert es die Übertragung eines einzelnen N-Acetylglucosamins von UDP-GlcNAc auf einen Serin- oder Threoninrest in zytoplasmatischen und nukleären Proteinen, was zu deren Modifikation mit einem β-verknüpften N-Acetylglucosamin (O-GlcNAc) führt (PubMed:26678539, PubMed:23103939, PubMed:21240259, PubMed:21285374, PubMed:15361863). Glykosyliert eine Vielzahl von Proteinen, darunter Histon H2B, AKT1, EZH2, PFKL, KMT2E/MLL5, MAPT/TAU und HCFC1. Es kann zelluläre Prozesse regulieren, indem es die Wechselwirkungen zwischen Glykosylierung und Phosphorylierung beeinflusst oder die proteolytische Prozessierung verändert (PubMed:21285374). Vermutlich stabilisiert es KMT2E/MLL5 durch Glykosylierung und Verhinderung seiner Ubiquitinierung (PubMed:26678539). Es ist an der Insulinresistenz in Muskel- und Fettzellen beteiligt, indem es Komponenten der Insulin-Signalübertragung glykosyliert, die Phosphorylierung von AKT1 an Thr-308 hemmt, die IRS1-Phosphorylierung verstärkt und die Insulin-Signalübertragung abschwächt (durch Ähnlichkeit). Es ist an der Regulation der Glykolyse beteiligt, indem es die Glykosylierung der 6-Phosphofructokinase PFKL vermittelt und deren Aktivität hemmt (PubMed:22923583). Es ist Bestandteil eines THAP1/THAP3-HCFC1-OGT-Komplexes, der für die Regulation der Transkriptionsaktivität von RRM1 erforderlich ist. Es spielt eine Schlüsselrolle in der Chromatin-Struktur, indem es die O-GlcNAcylierung von Ser-112 des Histons H2B vermittelt. Durch seine Interaktion mit TET-Proteinen (TET1, TET2 oder TET3) wird es an CpG-reiche Transkriptionsstartstellen aktiver Gene rekrutiert (PubMed:22121020, PubMed:23353889). Als Teil des NSL-Komplexes ist es indirekt an der Acetylierung des nukleosomalen Histons H4 an mehreren Lysinresten beteiligt (PubMed:20018852). Die O-GlcNAcylierung von Ser-75 in EZH2 erhöht dessen Stabilität und erleichtert die Bildung von H3K27me3 durch den PRC2/EED-EZH2-Komplex (PubMed:24474760). Sie reguliert die zirkadiane Rhythmik der Uhrgene und die Glukosehomöostase in der Leber. Durch O-Glykosylierung stabilisiert sie die Uhrproteine ARNTL/BMAL1 und CLOCK, wodurch deren Ubiquitinierung und der anschließende Abbau verhindert werden. Fördert die CLOCK-ARNTL/BMAL1-vermittelte Transkription von Genen der negativen Schleife der circadianen Uhr, wie z. B. PER1/2 und CRY1/2 (PubMed:12150998, PubMed:19451179, PubMed:20018868, PubMed:20200153, PubMed:21285374, PubMed:15361863). O-glykosyliert HCFC1 und reguliert dessen proteolytische Prozessierung und Transkriptionsaktivität (PubMed:21285374, PubMed:28584052, PubMed:28302723). Reguliert die mitochondriale Motilität in Neuronen durch Glykosylierung von TRAK1 (ähnlich). Glykosyliert HOXA1 (ähnlich). O-Glykosyliert FNIP1 (PubMed:30699359). |