PHD3 (11Y3) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Mensch, Maus, Ratte
Genname
EGLN3
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | PHD3 (11Y3) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Mensch, Maus, Ratte |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | EGLN3 |
| alternative Namen | Egl nine homolog 3; EGLN3; Factor responsive smooth muscle protein; HIF Prolyl Hydroxylase 3; HIFP4H3; HIFPH3; P4H3; PHD3; SM20; |
| Gene ID | 112399 |
| SwissProt ID | Q9H6Z9 |
| Immunogen | Rekombinantes Protein des humanen PHD3 |
Anwendung
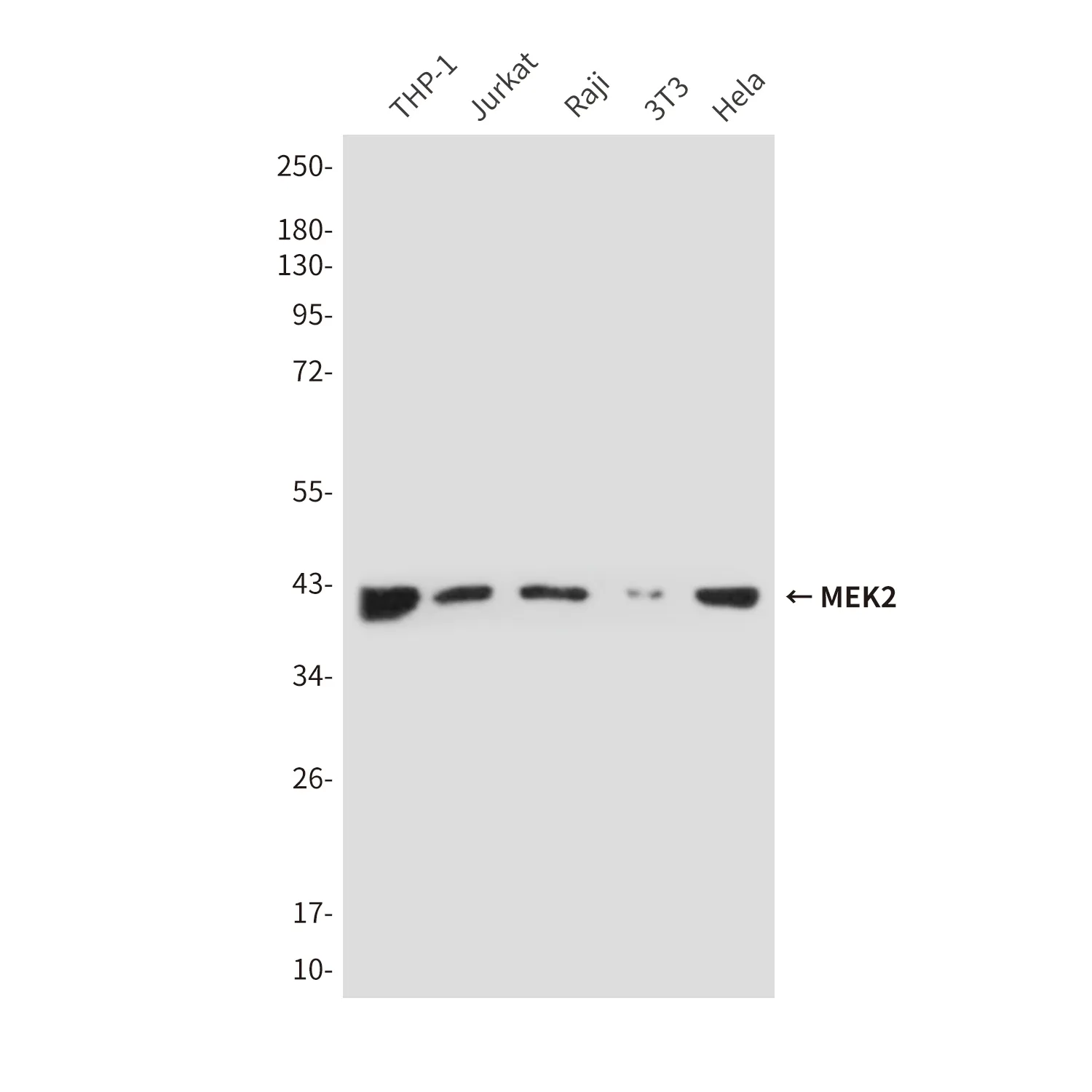
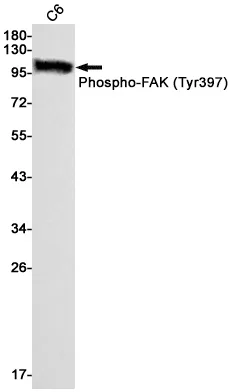
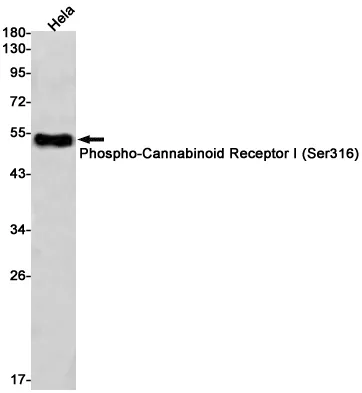
| Anwendung | WB,IHC,ICC/IF,IP |
| Verdünnungsverhältnis | WB 1:500-1:2000,IHC 1:50-1:100,ICC/IF 1:20-1:50,IP 1:20-1:50 |
| Molekulargewicht | 27kDa |
Forschungsgebiet
| Cardiovascular |
Hintergrund
| Katalysiert die posttranslationale Bildung von 4-Hydroxyprolin in Hypoxie-induzierbaren Faktor (HIF)-alpha-Proteinen. Hydroxyliert HIF-1α an Pro-564 und HIF-2α. Fungiert als zellulärer Sauerstoffsensor und markiert unter normoxischen Bedingungen HIF durch Hydroxylierung für den proteasomalen Abbau über den von-Hippel-Lindau-Ubiquitinierungskomplex. Prolylhydroxylase, die die Hydroxylierung von Prolinresten in Zielproteinen wie PKM, TELO2, ATF4 und HIF1A vermittelt (PubMed:19584355, PubMed:21620138, PubMed:21483450, PubMed:22797300, PubMed:20978507, PubMed:21575608). Zielproteine werden bevorzugt über ein LXXLAP-Motiv erkannt. Ein zellulärer Sauerstoffsensor, der unter normoxischen Bedingungen die posttranslationale Bildung von 4-Hydroxyprolin in Hypoxie-induzierbaren Faktor (HIF)-alpha-Proteinen katalysiert (PubMed:11595184, PubMed:12181324). Er hydroxyliert ein spezifisches Prolin in den sauerstoffabhängigen Degradationsdomänen (ODD) (N-terminal, NODD, und C-terminal, CODD) von HIF1A (PubMed:11595184, PubMed:12181324) und auch HIF2A (PubMed:11595184, PubMed:12181324). Er zeigt eine Präferenz für die CODD-Stelle sowohl von HIF1A als auch von HIF2A (PubMed:11595184, PubMed:12181324). Die Hydroxylierung an der NODD-Stelle durch EGLN3 scheint eine vorherige Hydroxylierung an der CODD-Stelle zu erfordern (PubMed:11595184, PubMed:12181324). Hydroxylierte HIFs werden anschließend über den von-Hippel-Lindau-Ubiquitinierungskomplex dem proteasomalen Abbau zugeführt (PubMed:11595184, PubMed:12181324). Unter hypoxischen Bedingungen ist die Hydroxylierungsreaktion abgeschwächt, wodurch die HIFs dem Abbau entgehen und in den Zellkern translozieren, Heterodimere mit HIF1B bilden und die Expression hypoxieinduzierbarer Gene erhöhen (PubMed:11595184, PubMed:12181324). ELGN3 ist das wichtigste Isoenzym zur Begrenzung der physiologischen Aktivierung von HIFs (insbesondere HIF2A) unter Hypoxie. Unter Hypoxie hydroxyliert es PKM und begrenzt dadurch die Glykolyse (PubMed:21620138, PubMed:21483450). Unter Normoxie hydroxyliert es ADRB2 und reguliert dessen Stabilität (PubMed:19584355). Es reguliert die Apoptose von Kardiomyozyten und Neuronen. In Kardiomyozyten hemmt es die antiapoptotische Wirkung von BCL2 durch Dissoziation des BAX-BCL2-Komplexes (PubMed:20849813). In Neuronen hat es eine NGF-induzierte proapoptotische Wirkung, vermutlich durch die Regulation der CASP3-Aktivität (PubMed:16098468). Es ist außerdem essenziell für die hypoxische Regulation der neutrophilen Entzündung (PubMed:21317538). Spielt eine entscheidende Rolle bei der DNA-Schadensantwort (DDR) durch Hydroxylierung von TELO2 und fördert dessen Interaktion mit ATR, die für die Aktivierung des ATR/CHK1/p53-Signalwegs erforderlich ist (PubMed:22797300). Vermittelt außerdem die Hydroxylierung von ATF4, was zu einer verringerten Proteinstabilität von ATF4 führt (wahrscheinlich). |