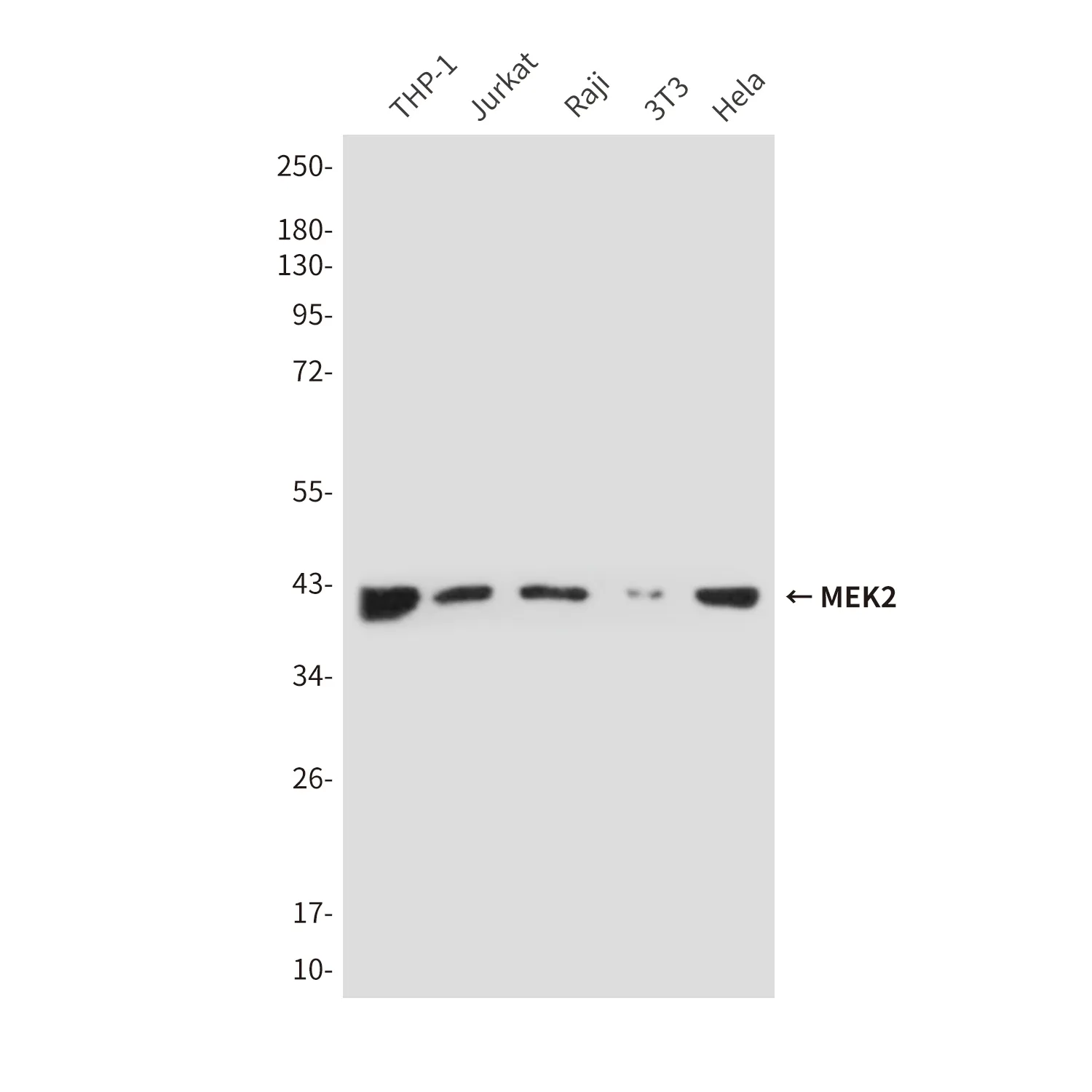
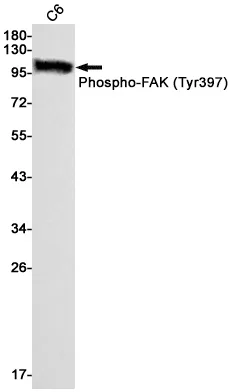
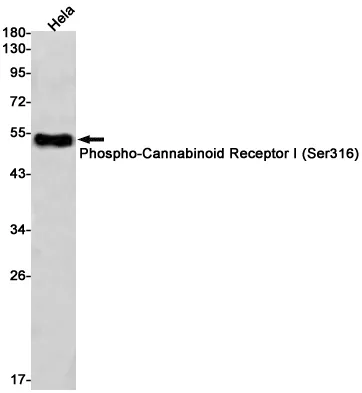
Phospho-AMPK alpha 2 (S491) (6K18) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Mensch, Maus, Ratte
Genname
PRKAA2
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | Phospho-AMPK alpha 2 (S491) (6K18) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Mensch, Maus, Ratte |
| Konjugation | Unkonjugiert |
| Modifikation | Phosphoryliert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | PRKAA2 |
| alternative Namen | 5'-AMP-activated protein kinase catalytic subunit alpha-2; ACACA kinase; Acetyl-CoA carboxylase kinase; AMPK alpha 2 chain; AMPK subunit alpha-2; AMPK2; AMPKalpha2; PRKAA2; |
| Gene ID | 5563 |
| SwissProt ID | P54646 |
| Immunogen | Ein synthetisches Phosphopeptid, das den Resten um Ser491 des humanen AMPK alpha 2 entspricht. |
Anwendung
| Anwendung | WB |
| Verdünnungsverhältnis | WB 1:500-1:2000 |
| Molekulargewicht | 62kDa |
Forschungsgebiet
| Neuroscience |
Hintergrund
| Die AMP-aktivierte Proteinkinase (AMPK) ist von Hefen über Pflanzen bis hin zu Tieren hochkonserviert und spielt eine Schlüsselrolle in der Regulation der Energiehomöostase. AMPK ist ein heterotrimerer Komplex, bestehend aus einer katalytischen α-Untereinheit und regulatorischen β- und γ-Untereinheiten, die jeweils von zwei oder drei verschiedenen Genen kodiert werden (α1, 2; β1, 2; γ1, 2, 3). Die katalytische Untereinheit der AMP-aktivierten Proteinkinase (AMPK) ist eine Energiesensor-Proteinkinase, die eine Schlüsselrolle in der Regulation des zellulären Energiestoffwechsels spielt. Als Reaktion auf einen Abfall des intrazellulären ATP-Spiegels aktiviert AMPK energieproduzierende Stoffwechselwege und hemmt energieverbrauchende Prozesse: Sie hemmt die Protein-, Kohlenhydrat- und Lipidsynthese sowie das Zellwachstum und die Zellproliferation. AMPK wirkt durch direkte Phosphorylierung von Stoffwechselenzymen und durch längerfristige Effekte über die Phosphorylierung von Transkriptionsregulatoren. Wirkt zudem als Regulator der Zellpolarität durch Umstrukturierung des Aktin-Zytoskeletts, vermutlich durch indirekte Aktivierung von Myosin. Reguliert die Lipidsynthese durch Phosphorylierung und Inaktivierung von Enzymen des Lipidstoffwechsels wie ACACA, ACACB, GYS1, HMGCR und LIPE; reguliert die Fettsäure- und Cholesterinsynthese durch Phosphorylierung der Acetyl-CoA-Carboxylase (ACACA und ACACB) bzw. der hormonsensitiven Lipase (LIPE). Reguliert die Insulin-Signalübertragung und die Glykolyse durch Phosphorylierung von IRS1, PFKFB2 und PFKFB3. Beteiligt an der Internalisierung des Insulinrezeptors/INSR (PubMed:25687571). AMPK stimuliert die Glukoseaufnahme im Muskel durch Erhöhung der Translokation des Glukosetransporters SLC2A4/GLUT4 zur Plasmamembran, möglicherweise durch Vermittlung der Phosphorylierung von TBC1D4/AS160. Reguliert die Transkription und die Chromatin-Struktur durch Phosphorylierung von Transkriptionsregulatoren des Energiestoffwechsels, wie z. B. CRTC2/TORC2, FOXO3, Histon H2B, HDAC5, MEF2C, MLXIPL/ChREBP, EP300, HNF4A, p53/TP53, SREBF1, SREBF2 und PPARGC1A. Wirkt als Schlüsselregulator der Glukosehomöostase in der Leber durch Phosphorylierung von CRTC2/TORC2, was zur Sequestrierung von CRTC2/TORC2 im Zytoplasma führt. Unter Stressbedingungen phosphoryliert es Serin-36 von Histon H2B (H2BS36ph), wodurch die Transkription gefördert wird. Wirkt als Schlüsselregulator von Zellwachstum und -proliferation durch Phosphorylierung von TSC2, RPTOR und ATG1/ULK1: Bei Nährstoffmangel reguliert es den mTORC1-Komplex negativ, indem es die RPTOR-Komponente des mTORC1-Komplexes phosphoryliert und TSC2 phosphoryliert und aktiviert. Ebenfalls bei Nährstoffmangel fördert es die Autophagie durch Phosphorylierung und Aktivierung von ATG1/ULK1. Dabei aktiviert es auch WDR45 (PubMed:28561066). AMPK reguliert zudem den zirkadianen Rhythmus durch die Phosphorylierung von CRY1, was zu dessen Destabilisierung führt. Es reguliert möglicherweise den Wnt-Signalweg durch Phosphorylierung von CTNNB1, was zu dessen Stabilisierung führt. Darüber hinaus phosphoryliert es CFTR, EEF2K, KLC1, NOS3 und SLC12A1. Spielt eine wichtige Rolle bei der differenziellen Regulation von Pro-Autophagie- (bestehend aus PIK3C3, BECN1, PIK3R4 und UVRAG oder ATG14) und Nicht-Autophagie-Komplexen (bestehend aus PIK3C3, BECN1 und PIK3R4) als Reaktion auf Glukosemangel. Kann den Nicht-Autophagie-Komplex durch Phosphorylierung von PIK3C3 hemmen und den Pro-Autophagie-Komplex durch Phosphorylierung von BECN1 aktivieren (ähnlich wie bei anderen Proteinen). |