ATP5A1 (11Q15) Kaninchen-monoklonaler Antikörper
Konjugation: Unkonjugiert
Rekombinanter monoklonaler Kaninchenantikörper
Anwendung
Reaktivität
Mensch, Maus, Ratte
Genname
ATP5F1A
Lagerung
Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles.
Zusammenfassung
| Produktname | ATP5A1 (11Q15) Kaninchen-monoklonaler Antikörper |
| Beschreibung | Rekombinanter monoklonaler Kaninchenantikörper |
| Wirt | Kaninchen |
| Reaktivität | Mensch, Maus, Ratte |
| Konjugation | Unkonjugiert |
| Modifikation | Unverändert |
| Isotyp | IgG |
| Klonalität | Monoklonal |
| Form | Flüssig |
| Konzentration | Unkonjugiert |
| Lagerung | Aliquot and store at -20°C (valid for 12 months). Avoid freeze/thaw cycles. |
| Versand | Eisbeutel. |
| Puffer | Kaninchen-IgG in phosphatgepufferter Kochsalzlösung (PBS), pH 7,4, 150 mM NaCl, 0,02 % Konservierungsmittel Typ N und 50 % Glycerin. Kurzfristig bei +4 °C lagern. Langfristig bei -20 °C lagern. Wiederholtes Einfrieren und Auftauen vermeiden. |
| Reinigung | Affinitätsreinigung |
Antigeninformation
| Genname | ATP5F1A |
| alternative Namen | Atp5a1; ATP5AL2; ATPM; hATP1; HEL-S-123m; MC5DN4; MOM2; |
| Gene ID | 498 |
| SwissProt ID | P25705 |
| Immunogen | Ein synthetisches Peptid des humanen ATP5A |
Anwendung
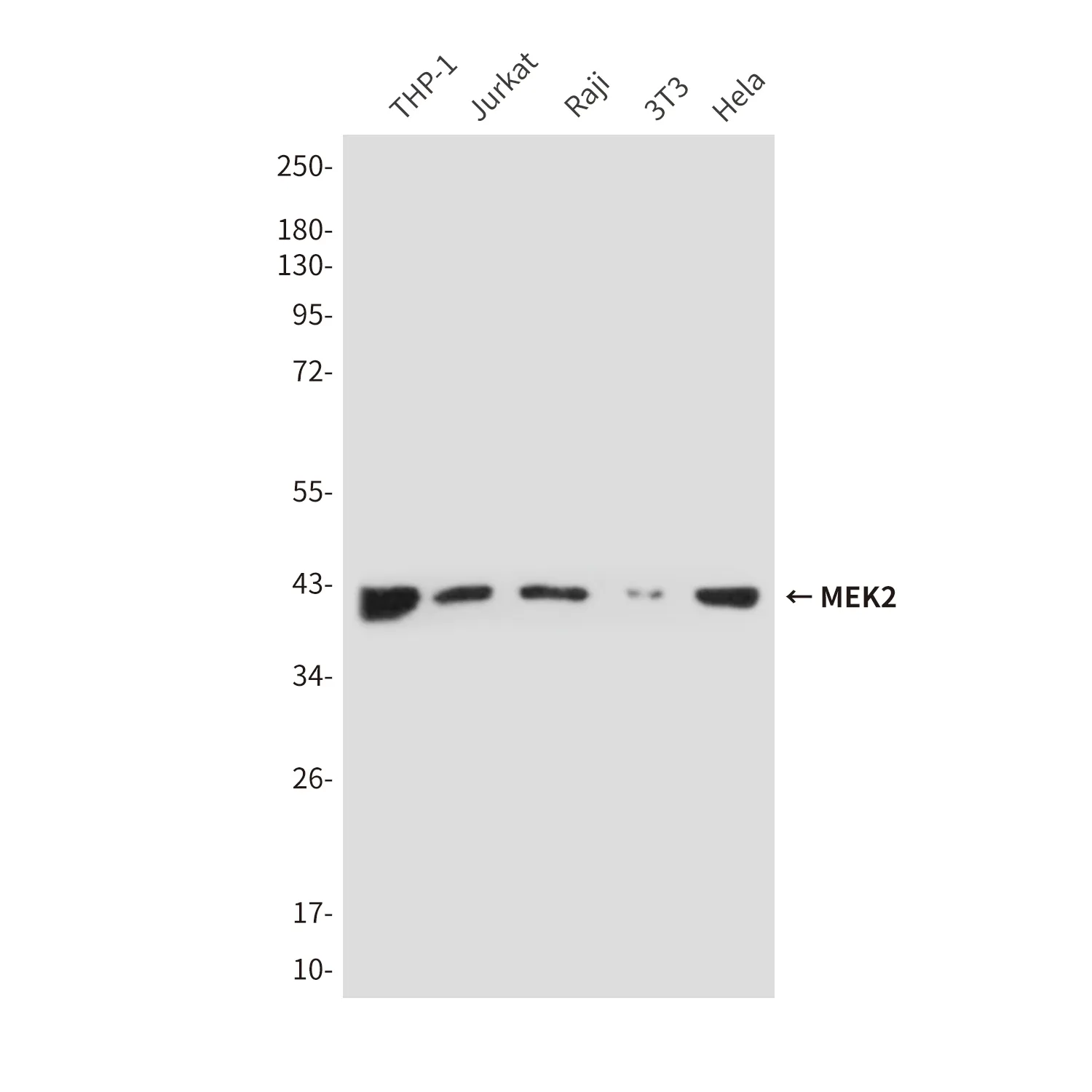
| Anwendung | WB,IHC,ICC/IF,FC |
| Verdünnungsverhältnis | WB 1:1000-1:5000,IHC 1:50-1:200,ICC/IF 1:100-1:200,FC 1:20-1:50 |
| Molekulargewicht | 60kDa |
Forschungsgebiet
| Mitochondria; ATPases; Mitochondrial markers; Complex V; Cancer |
Hintergrund
| Die mitochondriale Membran-ATP-Synthase (F1F0-ATP-Synthase oder Komplex V) produziert ATP aus ADP in Gegenwart eines Protonengradienten über die Membran, der durch die Elektronentransportkomplexe der Atmungskette erzeugt wird. F-Typ-ATPasen bestehen aus zwei Strukturdomänen: F1 – mit dem extramembranären katalytischen Kern – und F0 – mit dem Membranprotonenkanal. Diese sind durch einen zentralen und einen peripheren Stiel miteinander verbunden. Während der Katalyse ist die ATP-Synthese in der katalytischen Domäne von F(1) über einen Rotationsmechanismus der zentralen Stieluntereinheiten an die Protonentranslokation gekoppelt. Die Untereinheiten α und β bilden den katalytischen Kern von F(1). Die Rotation des zentralen Stiels relativ zu den umgebenden α₃β₃-Untereinheiten führt zur Hydrolyse von ATP an drei separaten katalytischen Zentren der β-Untereinheiten. Die Untereinheit α besitzt keine katalytischen ATP-Bindungsstellen mit hoher Affinität (aus Ähnlichkeit). Sie bindet das bakterielle Siderophor Enterobactin und kann die mitochondriale Akkumulation von Enterobactin-abgeleiteten Eisenionen fördern (PubMed:30146159). |